Il glucosio-6-fosfato (G6P) è un metabolita chiave del metabolismo dei carboidrati e, più in generale, del metabolismo cellulare.[1]
Nelle cellula animali e batteriche deriva principalmente dalla reazione catalizzata dall’enzima esochinasi, che catalizza il primo passaggio della via glicolitica. In alternativa, può essere prodotto attraverso la glicogenolisi, processo catabolico mediante il quale il glicogeno viene degradato per fornire glucosio in risposta a specifiche necessità metaboliche.[2] Una terza via di sintesi, sebbene quantitativamente meno rilevante, è rappresentata dalla conversione del galattosio attraverso la via di Leloir.[3]
Il glucosio-6-fosfato rappresenta un importante crocevia metabolico cellulare. A seconda delle esigenze, può proseguire lungo la glicolisi, essere convogliato nello shunt dell’esoso monofosfato, oppure essere utilizzato per la sintesi del glicogeno e nei processi di glicosilazione di macromolecole.[4] Inoltre, nel fegato, può essere convertito in glucosio libero o partecipare ai processi di detossificazione tramite glucuronazione.[5]
Indice
- Proprietà chimiche
- Vie di sintesi del glucosio-6-fosfato
- Perché la fosforilazione del glucosio a glucosio-6-fosfato è importante?
- Destino metabolico del glucosio-6-fosfato
- Bibliografia
Proprietà chimiche
Il glucosio-6-fosfato ha formula molecolare C6H13O9P e peso molecolare di 260,14 g/mol.
Secondo la nomenclatura IUPAC il suo nome è [(2R,3R,4S,5R)-2,3,4,5-tetraidrossi-6-ossoesil] diidrogeno fosfato.
Le sue costanti di dissociazione pKa1 e pKa2, a 25°C, sono pari a 1,65 e 6,11. Dunque a pH fisiologico si trova quasi esclusivamente in forma ionizzata e ha carica −2.[6]
Vie di sintesi del glucosio-6-fosfato
Nelle cellule animali e batteriche, escludendo la fotosintesi, il glucosio-6-fosfato viene prodotto principalmente attraverso due vie: la fosforilazione diretta del glucosio e, nelle cellule animali, la glicogenolisi. E inoltre possibile la sua sintesi dal galattosio.[2]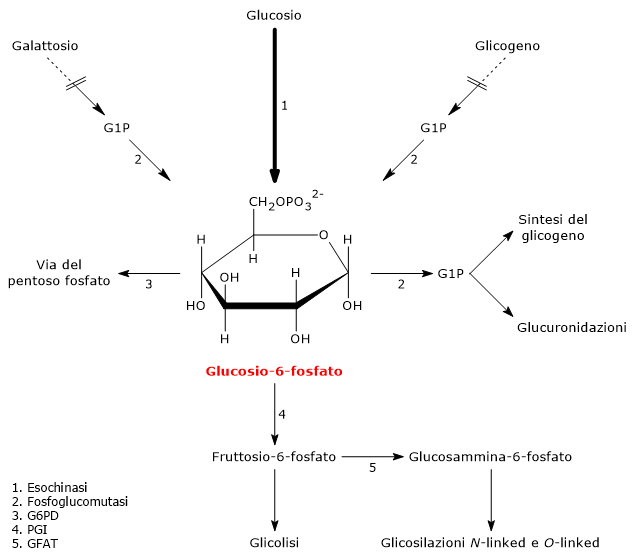
Esochinasi
Una volta entrato nella cellula, il principale destino metabolico del glucosio è la sua fosforilazione a glucosio-6-fosfato.
Questa reazione è la prima delle dieci che compongono la glicolisi ed è anche la prima delle due fosforilazioni cui il monosaccaride va incontro lungo tale via metabolica.
L’esochinasi (EC 2.7.1.1), un enzima presente nelle cellule di tutti gli organismi, e con quattro isoforme differenti nell’uomo, catalizza questa reazione irreversibile ossia la fosforilazione del glucosio a livello del C-6 a spese di una molecola di ATP.
Glucosio + ATP → Glucosio-6-fosfato + ADP + H⁺
La formazione del glucosio-6-fosfato è particolarmente rilevante quando il monosaccaride è disponibile dall’esterno, ad esempio dopo i pasti.[1]
Glicogenolisi
Il glucosio-6-fosfato può derivare anche dalla glicogenolisi, la via metabolica attraverso la quale le molecole di glucosio immagazzinate nel glicogeno, un polisaccaride, vengono liberate quando necessario.
Durante il digiuno, ad esempio di notte o nell’intervallo tra i pasti, ma anche nel corso dell’attività fisica, la glicogenolisi, a mezzo dell’intervento di tre attività enzimatiche, la glicogeno fosforilasi (EC 2.4.1.1), l’alfa-(1,4)-glucan-6-glicosiltransferasi (EC 2.4.1.25) e l’amilo-alfa-(1,6)-glucosidasi o enzima deramificante (EC 3.2.1.33), porta al rilascio di glucosio: circa il 90% in forma di glucoso-1-fosfato (G1P), e il restante 10% direttamente come glucosio.
Il glucosio-1-fosfato viene di seguito isomerizzato a glucosio-6-fosfato nella reazione, reversibile, catalizzata dalla fosfoglucomutasi (EC 5.4.2.2).[2]
Galattosio
Il galattosio è un monosaccaride presente nel latte e derivati dove si trova principalmente come componente, con il glucosio, del lattosio. Nella cellula, la principale via per il metabolismo del galattosio è la via di Leloir.[7]
A partire dal monosaccaride, la via di Leloir permette la formazione di metaboliti che potranno entrare in numerosi processi biochimici, sia anabolici che catabolici, a seconda del tessuto e delle condizioni metaboliche della cellula. Tra i possibili destini del galattosio lungo questa via c’è anche la conversione a glucosio-1-fosfato, che potrà quindi essere isomerizzato a glucosio-6-fosfato per essere indirizzato verso la glicolisi e la gluconeogenesi, o essere utilizzato nella sintesi del glicogeno.[3]
Perché la fosforilazione del glucosio a glucosio-6-fosfato è importante?
La fosforilazione del glucosio a glucosio-6-fosfato è metabolicamente importante per diverse ragioni.
- Il glucosio è una molecola neutra il cui passaggio attraverso la membrana plasmatica avviene per diffusione facilitata mediata da specifici trasportatori proteici appartenenti alla famiglia di proteine di trasporto di membrana GLUT o SLC2A.[8]
La fosforilazione sul C-6 conferisce al monosaccaride una carica negativa che gli impedisce di attraversare la membrana, anche per l’assenza di trasportatori specifici per zuccheri fosforilati. Dunque la fosforilazione intrappola il glucosio nella cellula.[4] - Grazie all’iniziale fosforilazione sul C-6 e all’assenza di trasportatori per gli zuccheri fosforilati non è più necessario spendere ulteriore energia per trattenere il glucosio-6-fosfato all’interno della cellula, nonostante la grande differenza esistente tra le sue concentrazioni intra- ed extracellulari.[9]
- La rapida conversione del glucosio in glucosio-6-fosfato contribuisce anche a mantenere bassa la concentrazione intracellulare di glucosio, agevolando così il suo ingresso per diffusione facilitata.[4]
- L’aggiunta di un gruppo fosfato aumenta il contenuto in energia della molecola, ossia inizia a destabilizzarla, facilitandone il successivo metabolismo.[9]
Destino metabolico del glucosio-6-fosfato
Il glucosio-6-fosfato rappresenta un punto di snodo centrale nel metabolismo dei carboidrati. Essendo un intermedio comune a diversi percorsi metabolici, il suo destino dipende dalle necessità metaboliche della cellula. Può infatti entrare in differenti vie metaboliche, sia anaboliche che cataboliche, quali la glicolisi, la gluconeogenesi, la via del pentoso fosfato, la sintesi del glicogeno, e la via delle esosammine. E’ infine coinvolto anche in quei processi di detossificazione che comportano la glucuronazione delle molecole da eliminare dall’organismo.[10]
Glicolisi
La glicolisi è una via metabolica fondamentale, non solo per la produzione di energia ma anche come fonte di intermedi per altre vie metaboliche.[11]
Il glucosio-6-fosfato può proseguire lungo la via, divenendo substrato della reazione catalizzata dalla fosfoglucosio isomerasi o glucosio-6-fosfato isomerasi (PGI; EC 5.3.1.9). L’enzima catalizza la sua isomerizzazione reversibile a fruttosio-6-fosfato, un esempio di isomeria di gruppo funzionale. Il fruttosio-6-fosfato non è tuttavia un metabolita esclusivo della glicolisi.
Nella terza reazione della via glicolitica il fruttosio-6-fosfato va incontro ad una seconda fosforilazione a dare fruttosio-1,6-bisfosfato. La reazione, catalizzata dalla fosfofruttochinasi-1 (PFK-1; EC 2.7.1.11), è irreversibile e porta alla formazione di un metabolita esclusivo della glicolisi e, in direzione opposta, della gluconeogenesi.[9]
Via delle esosammine
Il fruttosio-6-fosfato, prodotto dall’isomerizzazione del glucosio-6-fosfato, è uno dei substrati chiave della via delle esosammine. Questa via metabolica interessa circa il 2–5% del metabolismo del glucosio ed è essenziale per i processi di glicosilazione delle macromolecole.[10]
Nel primo passaggio, il fruttosio-6-fosfato viene convertito in glucosammina-6-fosfato nella reazione catalizzata dall’enzima glutammina:fruttosio-6-fosfato aminotransferasi (GFAT; EC 2.6.1.16), che catalizza la prima tappa di comando dell’intera via. In questa reazione l’amminoacido glutammina funge da donatore del gruppo amminico.[12]
I passaggi successivi portano infine alla sintesi della l’UDP-N-acetilglucosammina (UDP-GlcNAc), che è utilizzata nella glicosilazione N-linked e O-linked di proteine, lipidi e acidi nucleici.[13]
Via del pentoso fosfato
Il glucosio-6-fosfato può entrare nella via del pentoso fosfato o shunt dell’esoso monofosfato, un’alternativa alla glicolisi per il metabolismo ossidativo del glucosio.[14]
L’ingresso nello shunt avviene a livello della reazione catalizzata dalla glucosio-6-fosfato deidrogenasi (G6PD; EC 1.1.1.49). La reazione ne comporta l’ossidazione a 6-fosfoglucono-δ-lattone, che prosegue quindi lungo la via metabolica.
Lo shunt dell’esoso monofosfato ha una duplice funzione: la sintesi, in rapporti variabili a seconda delle condizioni metaboliche della cellula, di NADPH e ribosio-5-fosfato.
- Il NADPH è un coenzima ridotto fondamentale per le reazioni biosintetiche, ad esempio la sintesi degli acidi grassi e del colesterolo, come anche per la difesa antiossidante a mezzo della riduzione del glutatione ossidato.[1]
- Il ribosio-5-fosfato, uno zucchero a cinque atomi di carbonio, indispensabile per la sintesi dei nucleotidi e degli acidi nucleici, che risulta quindi molto importante durante le fasi di crescita.[4]
Si stima che oltre il 10% del glucosio metabolizzato venga convogliato attraverso questa via che, interessante da notare, pur ossidando il monosaccaride, non porta né alla produzione né al consumo di ATP.[15]
Sintesi del glicogeno
Il glucosio-6-fosfato può essere utilizzato per il ripristino delle riserve cellulari di glicogeno. La via anabolica che porta alla sintesi del polisaccaride si verifica quando sono disponibili carboidrati, la domanda di glucosio è bassa, e c’è un surplus energetico. La glicogenosintesi è particolarmente importante nel fegato e nel muscolo.[16]
Nel corso della sintesi del glicogeno, il glucosio-6-fosfato è isomerizzato a glucosio-1-fosfato nella reazione catalizzata dalla fosfoglucomutasi. L’enzima interviene anche nella glicogenolisi catalizzando però la reazione inversa. La direzione della reazione è determinata dalle concentrazioni relative dei due zuccheri fosforilati.
Nel passaggio successivo, lo scheletro carbonioso viene attivato a seguito del trasferimento di un UDP nella reazione catalizzata dalla UDP-glucosio pirofosforilasi (EC 2.7.7.9).
L’UDP-glucosio prodotto è quindi substrato della reazione catalizzata dalla glicogeno sintasi (EC 2.4.1.11) e utilizzato per allungare le catene del glicogeno. L’UDP-glucosio viene utilizzato come donatore di zuccheri anche nella sintesi dei glicolipidi.[4]
Processi di detossificazione
I processi di detossificazione permettono l’eliminazione di xenobiotici, farmaci e prodotti del catabolismo, come la bilirubina. Sono vie metaboliche che avvengono principalmente nel fegato, e in esse il glucosio-6-fosfato ha il ruolo di precursore nella sintesi dell’acido glucuronico.[17]
G6P, analogamente a quanto accade nella sintesi del glicogeno, viene prima attivato a UDP-glucosio. L’UDP-glucosio è quindi ossidato a UDP-glucuronato nella reazione catalizzata dalla UDP-glucosio 6-deidrogenasi (EC 1.1.1.22). L’UDP-glucuronato funge da donatore di acido glucuronico in reazioni catalizzate da UDP-glucuronosiltransferasi (EC 2.4.1.17). Il processo, definito glucuronidazione, aumenta l’idrofilicità di composti altrimenti lipofilici, facilitandone l’eliminazione con la bile o l’urina.[5]
Bibliografia
- ^ a b c Nelson D.L., Cox M.M. Lehninger. Principles of biochemistry. 6th Edition. W.H. Freeman and Company, 2012.
- ^ a b c Voet D. and Voet J.D. Biochemistry. 4th Edition. John Wiley J. & Sons, Inc. 2011.
- ^ a b Conte F., van Buuringen N., Voermans N.C., Lefeber D.J. Galactose in human metabolism, glycosylation and congenital metabolic diseases: time for a closer look. Biochim Biophys Acta Gen Subj 2021;1865(8):129898. doi:10.1016/j.bbagen.2021.129898
- ^ a b c d e Garrett R.H., Grisham C.M. Biochemistry. 4th Edition. Brooks/Cole, Cengage Learning, 2010.
- ^ a b Rowland A., Miners J.O., Mackenzie P.I. The UDP-glucuronosyltransferases: their role in drug metabolism and detoxification. Int J Biochem Cell Biol 2013;45(6):1121-32. doi:10.1016/j.biocel.2013.02.019
- ^ National Center for Biotechnology Information. PubChem Compound Summary for CID 439958, Glucose-6-Phosphate. https://pubchem.ncbi.nlm.nih.gov/compound/D-Glucose-6-phosphate. Accessed Apr. 19, 2025.
- ^ Leloir L.F., de Fekete M.A., Cardini C.E. Starch and oligosaccharide synthesis from uridine diphosphate glucose. J Biol Chem 1961;236:636-41. doi:10.1016/S0021-9258(18)64280-2
- ^ Thorens B., Mueckler M. Glucose transporters in the 21st Century. Am J Physiol Endocrinol Metab 2010;298(2):E141-5. doi:10.1152/ajpendo.00712.2009
- ^ a b c Berg J.M., Tymoczko J.L., and Stryer L. Biochemistry. 5th Edition. W. H. Freeman and Company, 2002.
- ^ a b Rajas F., Gautier-Stein A., Mithieux G. Glucose-6 phosphate, a central hub for liver carbohydrate metabolism. Metabolites 2019;9(12):282. doi:10.3390/metabo9120282
- ^ Kierans S.J., Taylor C.T. Glycolysis: a multifaceted metabolic pathway and signaling hub. J Biol Chem 2024;300(11):107906. doi:10.1016/j.jbc.2024.107906
- ^ Milewski S. Glucosamine-6-phosphate synthase—the multi-facets enzyme. Biochim Biophys Acta 2002;1597(2):173-92. doi:10.1016/s0167-4838(02)00318-7
- ^ Paneque A., Fortus H., Zheng J., Werlen G., Jacinto E. The hexosamine biosynthesis pathway: regulation and function. Genes (Basel) 2023;14(4):933. doi:10.3390/genes14040933
- ^ Horecker B.L. The pentose phosphate pathway. J Biol Chem 2002;277(50):47965-47971. doi:10.1074/jbc.X200007200
- ^ Michal G., Schomburg D. Biochemical pathways. An atlas of biochemistry and molecular biology. 2nd Edition. John Wiley J. & Sons, Inc. 2012.
- ^ Adeva-Andany M.M., González-Lucán M., Donapetry-García C., Fernández-Fernández C., Ameneiros-Rodríguez E. Glycogen metabolism in humans. BBA Clin 2016;5:85-100. doi:10.1016/j.bbacli.2016.02.001
- ^ Yang G., Ge S., Singh R., Basu S., Shatzer K., Zen M., Liu J., Tu Y., Zhang C., Wei J., Shi J., Zhu L., Liu Z., Wang Y., Gao S., Hu M. Glucuronidation: driving factors and their impact on glucuronide disposition. Drug Metab Rev 2017;49(2):105-138. doi:10.1080/03602532.2017.1293682