L’acido caproico è un acido grasso saturo con una catena alifatica lineare formata da sei atomi di carbonio.[8]
Isolato per la prima volta dal burro da Chevreul M.E. nel 1816, deve il suo nome all’odore che ricorda quello delle capre, in latino caper.[7]
Presente soprattutto nei prodotti caseari, in particolare in quelli derivati dal latte di capra, non si ritrova in forma libera ma piuttosto come componente dei trigliceridi.[3]
Nell’intestino, una volta rilasciato dai trigliceridi, grazie alla sua capacità di attraversare le membrane cellulari tramite diffusione passiva viene rapidamente assorbito e, a mezzo del circolo portale, trasportato al fegato, dove è altrettanto rapidamente metabolizzato a fini energetici.[2] Questa caratteristica ne fa un componente importante per la nutrizione di soggetti con specifici fabbisogni energetici.[1]
Nei mammiferi, l’acido caproico oltre a essere assunto con la dieta, può essere sintetizzato, soprattutto nel fegato, tramite processi di beta-ossidazione a carico di acidi grassi con catena più lunga, o de novo nella ghiandola mammaria dopo il parto.[3][9]
L’acido caproico trova applicazioni in vari settori, tra cui quelli alimentare, farmaceutico, zootecnico ed energetico.[4][13][14]
Indice
- Proprietà
- Fonti alimentari
- Assorbimento intestinale
- Trasporto
- Biosintesi
- Applicazioni industriali
- Bibliografia
Proprietà
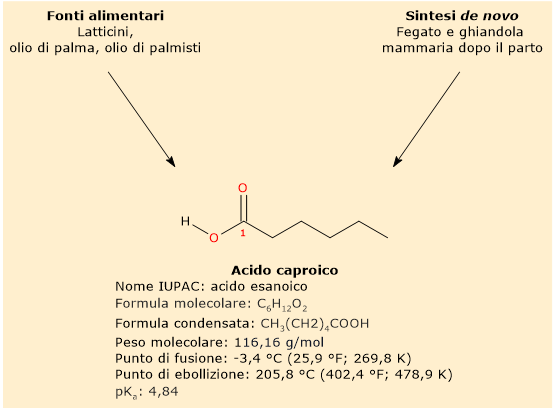
L’acido caproico ha un peso molecolare di 116,16 g/mol, formula molecolare C6H12O2, formula condensata CH3(CH2)4COOH, e abbreviazione 6:0. Secondo la nomenclatura IUPAC il suo nome è acido esanoico.[8]
E’ leggermente solubile in acqua mentre risulta solubile in etanolo.[14]
A temperatura ambiente si presenta come un liquido oleoso incolore o giallo, con un odore pungente che ricorda quello delle capre. Il suo punto di fusione è pari a -3,4 °C (25,9 °F; 269,8 K), mentre il punto di ebollizione è pari a 205,8 °C (402,4 °F; 478,9 K).[8]
La sua base coniugata è detta ione esanoato o caproato, ha formula condensata CH3(CH2)4COO–, ed è la forma con cui, a pH fisiologico, l’acido grasso libero si ritrova nei sistemi biologici, avendo un pKa di 4,84.[12]
 L’acido caproico fornisce circa 7,5 kcal/g.[1]
L’acido caproico fornisce circa 7,5 kcal/g.[1]
L’assenza di doppi legami nella catena carboniosa pone l’acido caproico nel gruppo degli acidi grassi saturi, e, poiché il numero di atomi di carbonio della catena è pari a 6, può esser inserito anche nel gruppo degli acidi grassi a catena media o MCFA, acidi grassi che hanno da 6 a 12 atomi di carbonio nella catena carboniosa.[1]
Nei trigliceridi è esterificato in prevalenza in posizione sn-3.[1]
Durante la stagionatura del formaggio, una piccola quantità di trigliceridi sono idrolizzati con conseguente liberazione di acidi grassi tra i quali gli acidi butirrico, caproico, caprilico e caprico contribuiscono all’aroma del prodotto.[3]
Fonti alimentari
L’acido caproico si trova in vari alimenti, in particolare quelli ricchi di grassi e oli, sebbene in quantità limitate, spesso inferiori al grammo per cento grammi di prodotto.
La principale fonte è rappresentata dai prodotti caseari come latte, burro, formaggi e panna. Tra i prodotti caseari risulta essere più abbondante nel latte di capra e nei formaggi derivati.[3]
Piccole quantità sono presenti anche nell’olio di cocco e nell’olio di palmisto.[12]
Nel grasso animale è presente in tracce.
Infine, l’acido caproico è uno dei tre acidi grassi presenti in alcuni oli MCT, ossia oli di trigliceridi a catena media.
Assorbimento intestinale
Al pari degli altri acidi grassi, anche l’acido caproico è presente quasi esclusivamente come componente dei trigliceridi, e quindi, per essere assorbito dovrà essere liberato.
Una volta rilasciato per idrolisi dal trigliceride, vista la sua leggera solubilità in ambiente acquoso, è in grado di superare la barriera d’acqua presente sulla superficie luminale degli enterociti.
Il passaggio attraverso la membrana plasmatica dell’enterocita, come delle altre membrane cellulari con cui viene in contatto, è indipendente dall’azione di specifiche proteine di trasporto, avviene per diffusione passiva e probabilmente interessa la forma protonata della molecola.[2] Ciò significa che anche l’ingresso nella matrice mitocondriale, dove sarà utilizzato a fini energetici, è indipendente dalla shuttle della carnitina, al pari degli altri MCFAs e degli acidi grassi a catena corta o SCFAs.
A que
ste modalità di trasporto si deve probabilmente l’elevata velocità con cui gli acidi grassi a catena corta e media sono metabolizzati, superiore a quella degli acidi grassi a catena lunga che invece necessitano di specifici carrier proteici.[10][11] Ed è per questo motivo che, con gli altri MCFAs, svolge un ruolo particolarmente importante nell’alimentazione dei bambini prematuri e dei soggetti affetti da malassorbimento dei grassi.[1]
Trasporto
La frazione di acido caproico non utilizzata dalla cellula intestinale non è incorporato nei chilomicroni ma passa direttamente nel circolo portale a mezzo del quale, per la maggior parte legata all’albumina, raggiunge il fegato, dove è assorbito quasi per intero e rapidamente metabolizzato.[12]
Non essendo incorporato nei chilomicroni, quindi bypassando il circolo linfatico e il successivo ingresso nella circolazione sistemica, e vista anche l’esigua quantità presente negli alimenti, è improbabile che l’acido caproico sia immagazzinato nel tessuto adiposo.
Biosintesi
Sebbene la principale fonte di acido caproico sia la dieta, questo acido grasso può essere sintetizzato anche nei tessuti dei mammiferi, e quindi degli esseri umani.
La sintesi avviene principalmente a livello epatico a mezzo di cicli di beta-ossidazione perossisomiale di acidi grassi, cicli durante i quali la catena carboniosa viene accorciata di due atomi di carbonio rispetto all’acido grasso in ingresso.[9] Di seguito una acil-CoA tioesterasi idrolizza il legame tioestere rilasciando l’acido grasso che può così raggiungere il citosol.[5]
L’acido caproico, con gli MCFA, è sintetizzato anche nella ghiandola mammaria, ma solo dopo il parto. L’analisi del secreto delle ghiandole mammarie prima del parto ha infatti evidenziato la presenza di lipidi in quantità decisamente inferiori rispetto al colostro e al latte.[3] Sembra quindi che il parto ne inneschi la sintesi.
Nella ghiandola mammaria la sintesi de novo degli acidi grassi con catena alifatica composta da 6 a 14 atomi di carbonio sembra avvenire grazie alla presenza della tioesterasi II (EC 3.1.2.20), enzima in grado di terminare l’allungamento della catena carboniosa prima del raggiungimento dei 16 atomi di carbonio, cosa che avviene in tutti gli altri tessuti, dove la tioesterasi I (EC 3.1.2.2) arresta la sintesi una volta prodotto l’acido palmitico.[6] Negli esseri umani, come in altre specie, il tasso di sintesi dell’acido caproico e degli altri MCFAs, aumenta con la durata dell’allattamento.[3]
Applicazioni industriali
L’acido caproico ha un’ampia gamma di applicazioni che spaziano dall’industria alimentare alla farmaceutica, fino ai settori energetico e zootecnico.
- Industria alimentare: è impiegato come aroma commestibile in spezie e additivo alimentare, ad esempio, nel burro e nel pane.
- Industria farmaceutica: viene utilizzato nella sintesi di farmaci come fonte del gruppo etile, ad esempio nella sintesi dell’acetato di zinco caproato, farmaco utilizzato nel trattamento delle ulcere gastriche, e nella sintesi dell’acido amino caproico, farmaco emostatico.[14]
- Zootecnia: è aggiunto ai mangimi animali come potenziale sostituto degli antibiotici, favorisce la salute intestinale e rafforza l’immunità.[4][13]
- Settore energetico: è un precursore per la produzione di biocarburanti, incluso gasolio e carburanti per l’aviazione, sebbene non sia utilizzabile direttamente come combustibile.[14]
Bibliografia
- ^ a b c d e Akoh C.C., Min D.B. Food lipids: chemistry, nutrition, and biotechnology. 3th Edition. 2008. doi:10.1201/9781420046649
- ^ a b Charney A.N., Micic L., Egnor R.W. Nonionic diffusion of short-chain fatty acids across rat colon. Am J Physiol 1998;274(3):G518-24. doi:10.1152/ajpgi.1998.274.3.G518
- ^ a b c d e f Chow C.K. Fatty acids in foods and their health implication. 3th Edition. 2008. doi:10.1201/9781420006902
- ^ a b Desbois A.P. Potential applications of antimicrobial fatty acids in medicine, agriculture and other industries. Recent Pat Antiinfect Drug Discov 2012;7(2):111-22. doi:10.2174/157489112801619728
- ^ Hunt M.C., Siponen M.I., Alexson S.E. The emerging role of acyl-CoA thioesterases and acyltransferases in regulating peroxisomal lipid metabolism. Biochim Biophys Acta 2012;1822(9):1397-410. doi:10.1016/j.bbadis.2012.03.009
- ^ Hunt M.C., Yamada J., Maltais L.J., Wright M.W., Podesta E.J., Alexson S.E. A revised nomenclature for mammalian acyl-CoA thioesterases/hydrolases. J Lipid Res 2005;46(9):2029-32. doi:10.1194/jlr.E500003-JLR200
- ^ Leray C. Contribution of Chevreul to lipid chemistry. OCL OILS FAT CROP LI 2023:30(9). doi:10.1051/ocl/2023006
- ^ a b c National Center for Biotechnology Information. PubChem Compound Summary for CID 8892, Caproic Acid. https://pubchem.ncbi.nlm.nih.gov/compound/Caproic-Acid. Accessed Dec. 22, 2024.
- ^ a b Nelson D.L., Cox M.M. Lehninger. Principles of biochemistry. 6th Edition. W.H. Freeman and Company, 2012.
- ^ Pégorier J.P., Duée P.H., Herbin C., Laulan P.Y., Bladé C., Peret J., Girard J. Fatty acid metabolism in hepatocytes isolated from rats adapted to high-fat diets containing long- or medium-chain triacylglycerols. Biochem J 1988;249(3):801-6. doi:10.1042/bj2490801
- ^ Roopashree P.G., Shetty S.S., Kumari N.S. Effect of medium chain fatty acid in human health and disease. J Funct Foods 2021;87:104724. doi:10.1016/j.jff.2021.104724
- ^ a b c Schönfeld P., Wojtczak L. Short- and medium-chain fatty acids in energy metabolism: the cellular perspective. J Lipid Res 2016;57(6):943-54. doi:10.1194/jlr.R067629
- ^ a b Van Immerseel F., De Buck J., Boyen F., Bohez L., Pasmans F., Volf J., Sevcik M., Rychlik I., Haesebrouck F., Ducatelle R. Medium-chain fatty acids decrease colonization and invasion through hilA suppression shortly after infection of chickens with Salmonella enterica serovar Enteritidis. Appl Environ Microbiol 2004;70(6):3582-7. doi:10.1128/AEM.70.6.3582-3587.2004
- ^ a b c d Yuan S., Jin Z., Ali A., Wang C., Liu J. Caproic acid-producing bacteria in chinese Baijiu brewing. Front Microbiol 2022;13:883142. doi:10.3389/fmicb.2022.883142